Mở đầu trang 10: Khoảng năm 440 trước Công Nguyên, nhà triết học Hy Lạp, Đê – mô – crit (Democritos) cho rằng: nếu chia nhỏ nhiều lần một đồng tiền vàng cho đến khi “không thể phân chia được nữa”, thì sẽ đuộc một hạt gọi là nguyên tử. (“Nguyên tử” trong tiếng Hy Lạp là atomos, nghiac là “không chia nhỏ hơn được nữa”). Vậy nguyên tử có phải hạt nhỏ nhất không?
Lời giải:
Nguyên tử không phải là hạt nhỏ nhất. Trong nguyên tử còn có các hạt: electron, proton, neutron
I. Nguyên tử là gì
Câu hỏi 1 trang 10: Hãy cho biết nguyên tử là gì
Lời giải:
Nguyên tử là những hạt cực kì nhỏ bé, không mang điện
Ví dụ: Đồng tiền vàng được cấu tạo từ nguyên tử vàng
Kim cương, than chì đều được cấu tạo từ nguyên tử carbon
Nước được tạo nên từ các nguyên tử hydrogen và oxygen
Câu hỏi 2 trang 10: Kể tên hai chất có chứa nguyên tử oxygen
Lời giải:
Hai chất có chứa nguyên tử oxygen là:
+ Khí oxygen được cấu tạo từ nguyên tử oxygen
+ Đường ăn được tạo nên từ các nguyên tử carbon, hydrogen và oxygen
II. Cấu tạo nguyên tử
Câu hỏi 3 trang 11: Trong các hạt cấu tạo nên nguyên tử:
a) Hạt nào mang điện tích âm?
b) Hạt nào mang điện tích dương?
c) Hạt nào không mang điện
Lời giải:
Trong các hạt cấu tạo nên nguyên tử:
a) Hạt electron (e) mang điện tích âm
b) Hạt proton (p) mang điện tích dương
c) Hạt neutron (n) không mang điện
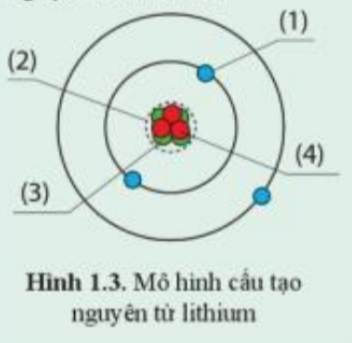
Luyện tập 1 trang 11: Quan sát hình 1.3 và hoàn thành thông tin chú thích các thành phần trong cấu tạo nguyên tử lithium
Lời giải:
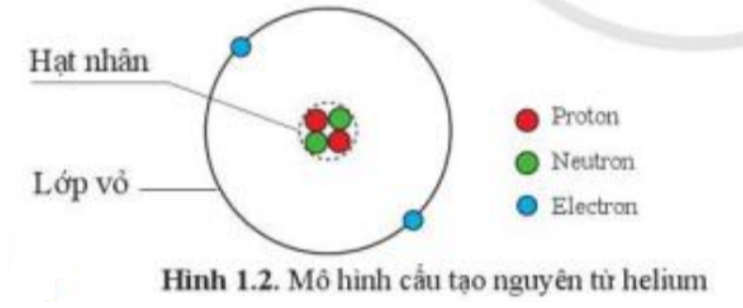
Quan sát hình 1.2 để hoàn thành hình 1.3
(1): Electron
(2): Hạt nhân
(3): Neutron
(4): Proton
Luyện tập 2 trang 11: Hoàn thành thông tin trong bảng sau:
| Nguyên tử | Số proton | Số neutron | Số electron | Điện tích hạt nhân |
| Hydrogen | 1 | 0 | ? | ? |
| Carbon | ? | 6 | 6 | ? |
| Nhôm | 13 | 14 | ? | ? |
Lời giải:
– Hydrogen có số proton = 1 => Số electron = 1 và điện tích hạt nhân = +1
– Carbon có số electron = 6 => Số proton = 6 => Điện tích hạt nhân = +6
– Nhôm có số proton = 13 => Số electron = 13 và điện tích hạt nhân = +13
Hoàn thành bảng
| Nguyên tử | Số proton | Số neutron | Số electron | Điện tích hạt nhân |
| Hydrogen | 1 | 0 | 1 | +1 |
| Carbon | 6 | 6 | 6 | +6 |
| Nhôm | 13 | 14 | 13 | +13 |
Luyện tập 3 trang 12: Nhôm (aluminium) là kim loại có nhiều ứng dụng trong thực tiễn, được dùng làm dây dẫn điện, chế tạo các thiết bị, máy móc trong công nghiệp và nhiều đồ dùng sinh hoạt. Cho biết tổng số hạt trong hạt nhân nguyên tử nhôm là 27, số đơn vị điện tích hạt nhân là 13. Tính số hạt mỗi loại trong nguyên tử nhôm và cho biết điện tích hạt nhân của nhôm
Lời giải:
– Vì hạt nhân gồm có proton và neutron
=> Tổng số hạt trong hạt nhân = số proton + số neutron
=> 27 = số proton + số neutron
– Mà số đơn vị điện tích hạt nhân = số proton = 13 = số electron
=> Số neutron = 27 – 13 = 14
Vậy trong nguyên tử nhôm có: 13 hạt electron, 13 hạt proton, 14 hạt neutron
Tìm hiểu thêm trang 12: Điện tích của nguyên tử helium bằng bao nhiêu?

Tổng điện tích trong nguyên tử helium bằng 0. Ta nói nguyên tử không mang điện hay trung hòa về điện
Cho biết nguyên tử lưu huỳnh (sulfur) có 16 electron. Hỏi nguyên tử lưu huỳnh có bao nhiêu proton? Hãy chứng minh nguyên tử lưu huỳnh trung hòa về điện
Lời giải:
– Vì trong nguyên tử, số electron = số proton
=> Số proton trong nguyên tử lưu huỳnh = 16
– Xét nguyên tử lưu huỳnh, ta có:
+ 16 proton, mỗi proton có điện tích +1 => Tổng số điện tích: +12
+ Neutron không mang điện => Tổng số điện tích: 0
+ 16 eletron, mỗi electronn có điện tích -1 => Tổng số điện tích: -12
=> Tổng điện tích của nguyên tử lưu huỳnh = (+12) + 0 + (-12) = 0
=> Nguyên tử lưu huỳnh trung hòa về điện
III. Sự chuyển động của electron trong nguyên tử
Câu hỏi 4 trang 12: Quan sát hình 1.4, hãy cho biết nguyên tử natri có bao nhiêu lớp electron. Mỗi lớp có bao nhiêu electron?
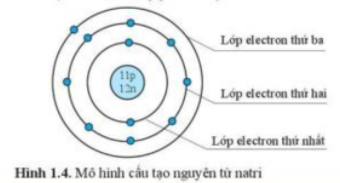
Lời giải:
– Trong hình 1.4 có
+ 3 vòng tròn => Natri có 3 lớp electron
+ 11 chấm xanh => Natri có 11 electron
Luyện tập 4 trang 13: Nguyên tử nitrogen và silicon có số electron lần lượt là 7 e và 14 e. Hãy cho biết nguyên tử nito và silicon có bao nhiêu lớp electron và có bao nhiêu electron ở lớp ngoài cùng
Lời giải:
– Xét nguyên tử nito có 7 electron: được phân bố thành 2 lớp electron, lớp thứ nhất có 2 electron, lớp thứ 2 có 5 electron
=> Ta nói nguyên tử nito có 5 electron ở lớp ngoài cùng
– Xét nguyên tử silicon có 14 electron được phân bố thành 3 lớp electron, lớp thứ nhất có 2 electron, lớp thứ 2 có 8 electron, lớp thứ 3 có 4 electron
=> Ta nói nguyên tử silicon có 4 electron ở lớp ngoài cùng
Luyện tập 5 trang 13: Quan sát hình ảnh mô tả cấu tạo nguyên tử carbon và nhôm (hình 1.5), hãy cho biết mỗi nguyên tử đó có bao nhiêu lớp electron và số electron trên mỗi lớp electron đó.
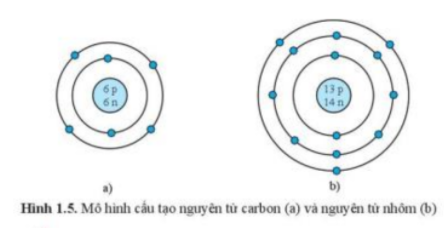
Lời giải:
– Xét hình 1.5a (nguyên tử carbon) ta có:
+ Có 2 vòng tròn => Nguyên tử carbon có 2 lớp electron
+ Vòng tròn thứ nhất có 2 chấm xanh => Lớp thứ nhất có 2 electron
+ Vòng tròn thứ 2 có 4 chấm xanh => Lớp thứ 2 có 4 electron
– Xét hình 1.5b (nguyên tử nhôm) ta có:
+ Có 3 vòng tròn => Nguyên tử nhôm có 3 lớp electron
+ Vòng tròn thứ nhất có 2 chấm xanh => Lớp thứ nhất có 2 electron
+ Vòng tròn thứ 2 có 8 chấm xanh => Lớp thứ 2 có 8 electron
+ Vòng tròn thứ 3 có 3 chấm xanh => Lớp thứ 3 có 3 electron
IV. Khối lượng nguyên tử
Câu hỏi 5 trang 13: Trong ba loại hạt tạo nên nguyên tử, hạt nào có khối lượng nhỏ nhất?
Lời giải:
– Proton và neutron đều có khối lượng xấp xỉ bằng 1 amu
– Electron có khối lượng là 0,00055 amu
=> Hạt electron có khối lượng nhỏ nhất
Câu hỏi 6 trang 13: Khối lượng của nguyên tử được tính bằng đơn vị nào?
Lời giải:
Khối lượng của nguyên tử được tính bằng đơn vị amu
Luyện tập 6 trang 13: Quan sát hình 1.5, hãy cho biết:
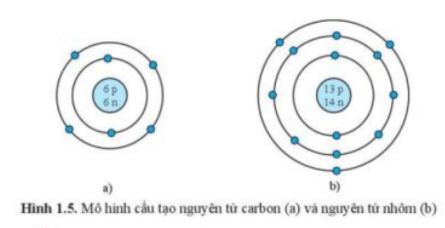
a) Số proton, neutron, electron trong mỗi nguyên tử carbon và nhôm
b) Khối lượng nguyên tử của carbon và nhôm
Lời giải:
a)
– Xét hình 1.5a (nguyên tử carbon) ta có:
+ 6p => Nguyên tử carbon có 6 proton và 6 electron
+ 6n => Nguyên tử carbon có 6 neutron
– Xét hình 1.5b (nguyên tử nhôm) ta có:
+ 13p => Nguyên tử carbon có 13 proton và 13 electron
+ 14n => Nguyên tử carbon có 14 neutron
b)
– Khối lượng nguyên tử có thể coi = khối lượng hạt nhân
– Hạt nhân gồm: proton và neutron
=> Khối lượng nguyên tử = số proton.1 + số neutron.1
– Xét hình 1.5a (nguyên tử carbon) có 6 proton và 6 neutron
=> Khối lượng nguyên tử carbon = 6.1 + 6.1 = 12 amu
– Xét hình 1.5b (nguyên tử nhôm) có 13 proton và 14 neutron
=> Khối lượng nguyên tử nhôm = 13.1 + 14.1 = 27 amu
Luyện tập 7 trang 14: Hoàn thành thông tin còn thiếu theo bảng sau:
| Hạt trong nguyên tử | Khối lượng (amu) | Điện tích | Vị trí trong nguyên tử |
| Proton | ? | +1 | ? |
| Neutron | ? | ? | Hạt nhân |
| Electron | 0,00055 | ? | ? |
Lời giải:
| Hạt trong nguyên tử | Khối lượng (amu) | Điện tích | Vị trí trong nguyên tử |
| Proton | 1 | +1 | Hạt nhân |
| Neutron | 1 | 0 | Hạt nhân |
| Electron | 0,00055 | -1 | Vỏ |
Vận dụng trang 14: Ruột của bút chì thường được làm từ than chì và đất sét. Than chì được cấu tọa từ các nguyên tử carbon
a) Hãy ghi chú thích tên các hạt tương ứng trong hình vẽ mô tả cấu tạo nguyên tử carbon
b) Em hãy tìm hiểu ý nghĩa của các kí hiệu HB, 2B và 6B được ghi trên một số loại bút chì.
Lời giải:
a) Trong hình vẽ mô tả cấu tạo nguyên tử carbon:
– Quả cầu màu đỏ: Proton
– Quả cầu màu xanh lá cây: Neutron
– Quả cầu màu xanh da trời: Electron
b) “B” là loại bút chì mềm, “H” là loại bút chì rắn